基于仿生理念开发的生物蛋白胶水兼具粘附性能、良好的生物相容性以及广阔的医用前景。尽管目前已经取得了系列进展,但由于缺乏在分子水平上对黏附蛋白质的理性设计以及对提升胶水性能的作用机制缺乏深度理解,导致目前开发的人工合成蛋白无法完美重现天然黏附结构蛋白的内在特征,限制了胶水的性能提升和应用转化。
近日,清华大学化学系刘凯、张洪杰团队联合广州医科大学郭伟圣团队以及华东师大孙静等研究人员发展了分子工程驱动的新一代超强蛋白胶水体系。研究人员受分子工程启发,编码重组蛋白氨基酸序列获取高阳离子特性蛋白质。随后通过超分子组装方法,将高阳离子蛋白质分别与DNA和十二烷基苯磺酸钠(SDBS)复合形成凝聚体生物胶水。一方面,编码的精氨酸显著增强了复合物体系的多种超分子相互作用力,使其在多种基质上具有超强粘附力,剪切粘合强度最高达~21 MPa,并在大鼠模型上实现了内脏止血和组织再生。另一方面,由于编码蛋白质具有的高电荷性,该体系展示出优异的抗菌特性,最低抑菌浓度比临床用抗生素低几个数量级。相关成果发表在Advanced Materials期刊上。

分子工程蛋白胶制备
首先,通过分子工程向类弹性蛋白序列中定点引入精氨酸(R),重组蛋白(R-蛋白)在大肠杆菌表达系统中表达,包括R18、R36、R72和R144。此外,将赖氨酸(K)单元引入以产生K144对照蛋白。随后分别引入鲑鱼精DNA和十二烷基苯磺酸钠作为阴离子组分以形成基于凝聚体的生物胶水。光学显微镜下观察其形成了致密且分布均匀的液滴。
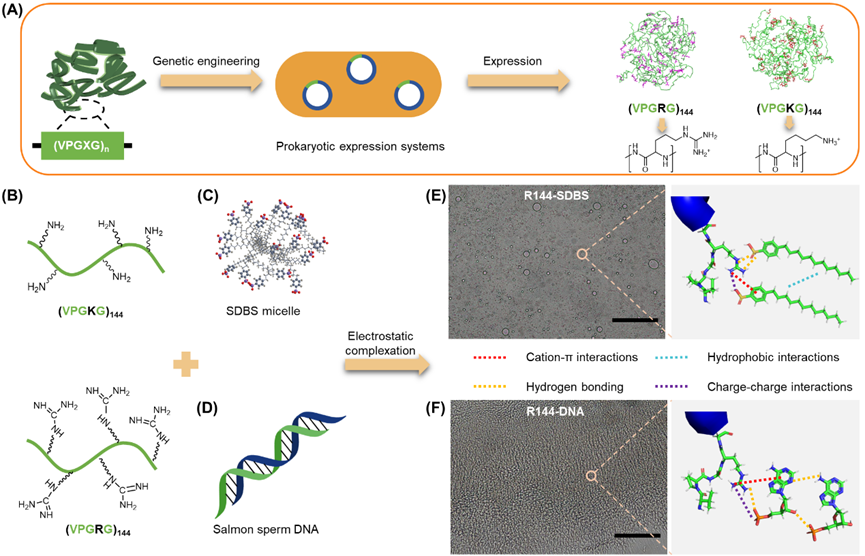
图:超强黏附蛋白胶水分子工程策略
生物胶水的性能测试
研究人员利用剪切粘合测试对胶水的粘附性能进行评价,发现其能牢固地粘附在高表面能材质上,显示出15.4-21.3MPa的剪切粘合强度。当应用于低能表面(例如PVC)时,粘附性能下降较为明显。这种行为可能归因于低表面能的材质不利于胶板之间形成多重相互作用力。随后,研究人员对胶水的含水量以及微观形态进行了表征。扫描电镜图像表明胶水均形成了高度交联和多孔的三维层状结构。
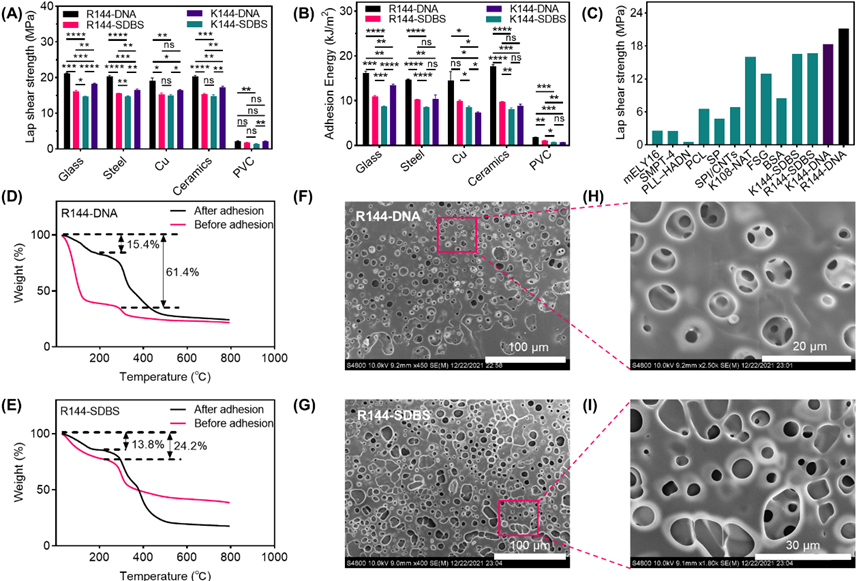
图:蛋白胶水性能表征
生物胶水的生物应用
鉴于强大的粘附性能、良好的生物相容性和生物降解性,研究人员对胶水的止血能力和组织愈合能力进行了探索。将胶水作用于出血的大鼠肝脏和肾脏上,伤口处的血液渗漏在10秒内迅速封闭,并且在基于凝聚层的胶中无肿胀现象。此外,在大鼠背部皮肤的线性伤口愈合试验中,治疗组的伤口在使用基于凝聚层的胶水第七天时几乎消失。然而,其他组表现出相对较慢的愈合速度和明显的疤痕,并且随后的组织学染色结果也证明治疗组拥有比其他组更少的炎症反应。
生物胶水的抗菌活性
基于系统中精氨酸的高质子化,重组蛋白表现出明显的抗菌性。对大肠杆菌ATCC25922和金黄色葡萄球菌ATCC25923的最低抑菌浓度相对较低证明了这一点。对于已建立的生物膜,其抗菌特性也得以保留。
小结
研究者通过分子工程创造了一类具有强大粘附性能的新型结构蛋白胶。该胶水是由从头设计的高阳离子蛋白质和带负电荷的分子基元通过静电组装制造而来。与赖氨酸序列相比,精氨酸的引入显著增加了多种超分子相互作用,例如阳离子-π和电荷-电荷相互作用。这种胶水材料由于其强大的粘附性、良好的生物相容性和卓越的抗菌能力,非常适合生物医学应用,例如内脏止血和组织再生。
以上文章转载于微信公众号高分子科学前沿,如有侵权,请及时联系我们修改或进行删除。

