寻找理想的骨再生性植入物仍然是临床上一个持续的挑战。天然骨组织的微观结构中,坚实的无机成分(羟基磷灰石)主要负责支撑、保护和承重,而柔软的有机成分(胶原纤维,多糖)在干细胞的增殖和迁移中起着重要作用。因此,有效地模拟天然骨软硬结合的杂化的结构与功能,有助于调控干细胞命运来改善骨再生进程。3D打印技术可以用于组织工程支架结构的精确控制,特别是创建有序孔隙和用户自定义结构,被广泛应用于组织工程领域。然而,目前以PCL,PLA等为主的挤出式3D打印支架难以提供组织重塑过程中长期稳定的营养供给,同时其表面缺乏活性配体,这会导致无效的细胞粘附和下游细胞事件,难以模拟骨组织再生过程所需的生理微环境。
针对以上问题,四川大学生物医学工程学院/国家生物医学材料工程技术研究中心孙勇研究员/樊渝江教授在前期的工作基础上(Nat. Commun., 2022; Adv. Funct. Mater., 2023),利用多巴胺介导的化学整合,将仿生胞外基质凝胶修饰在聚多巴胺涂层的3D打印PCL支架中,构建了软-硬结合的活性骨修复体(BM-g-DPCL,图1)。该策略改善了3D打印支架植入后的再生微环境,对于成骨基质的重塑起到重要作用。其中,梯度多孔结构设计有利于潜在的细胞迁移和营养传质;聚多巴胺涂覆的“硬”性PCL支架促进钙离子螯和及随后的类骨质沉积,并维持植入体的力学环境;多酚基团化学锚定的“软”性凝胶基质改善再生微环境,增强了干细胞的粘附、增殖和成骨分化。活性骨修复体(BM-g-DPCL)加速内源性干细胞(ESCs)募集,并启动了快速的血管形成(图2)。在兔颅骨缺损模型(Φ = 10 mm)中,活性支架促进新生组织与植入体界面融合,诱导新生骨基质在支架内部沉积(图3)。蛋白质组学确认细胞因子粘附、生物矿化沉积、快速血管化及促进胞外基质形成是加速骨缺损愈合的主要因素(图4)。这种仿生的软硬组分高度化学键和的策略提供了无细胞/无因子的组织工程支架再生的新策略。
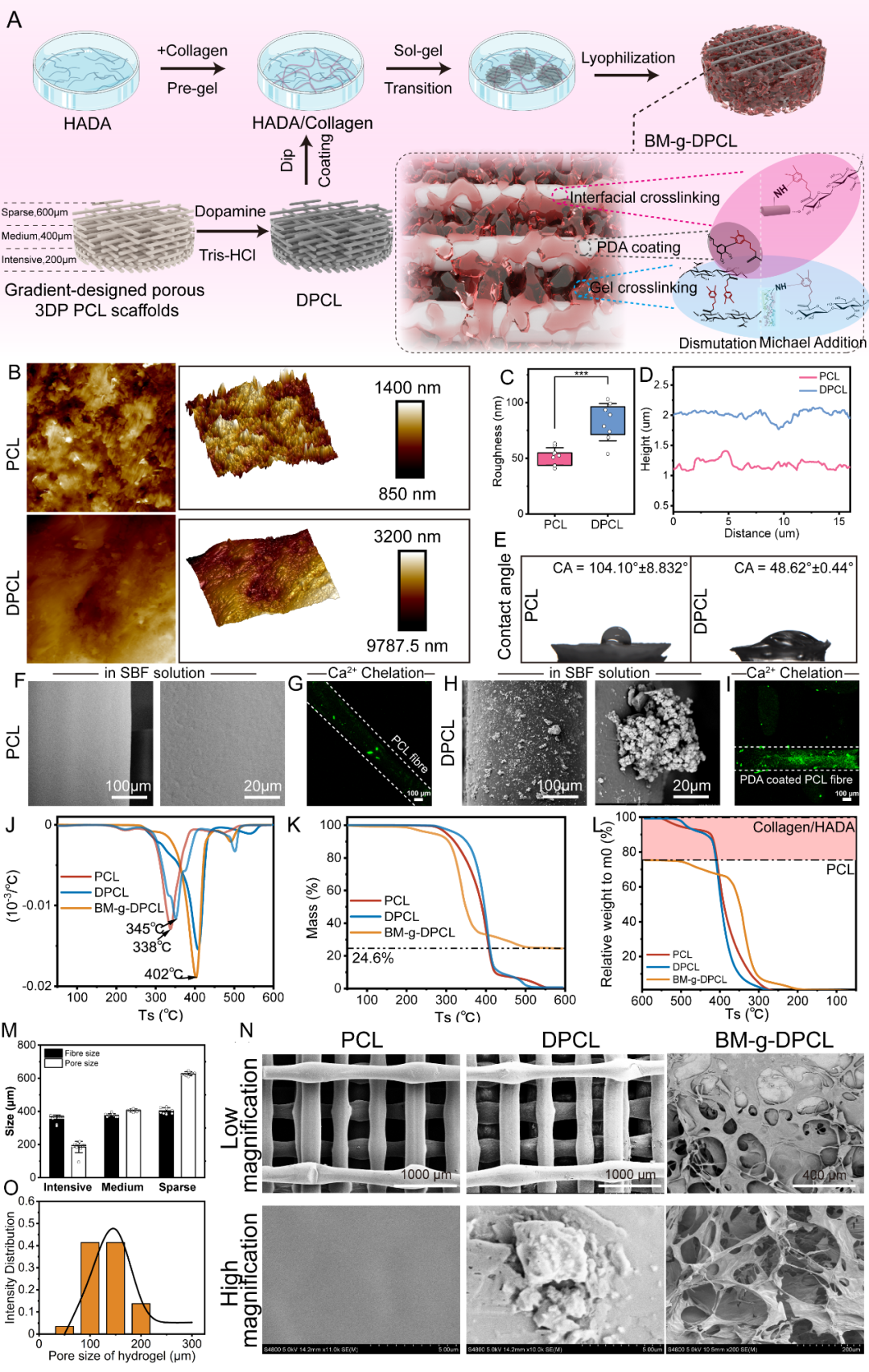
图1 活性骨修复体BM-g-DPCL的构建
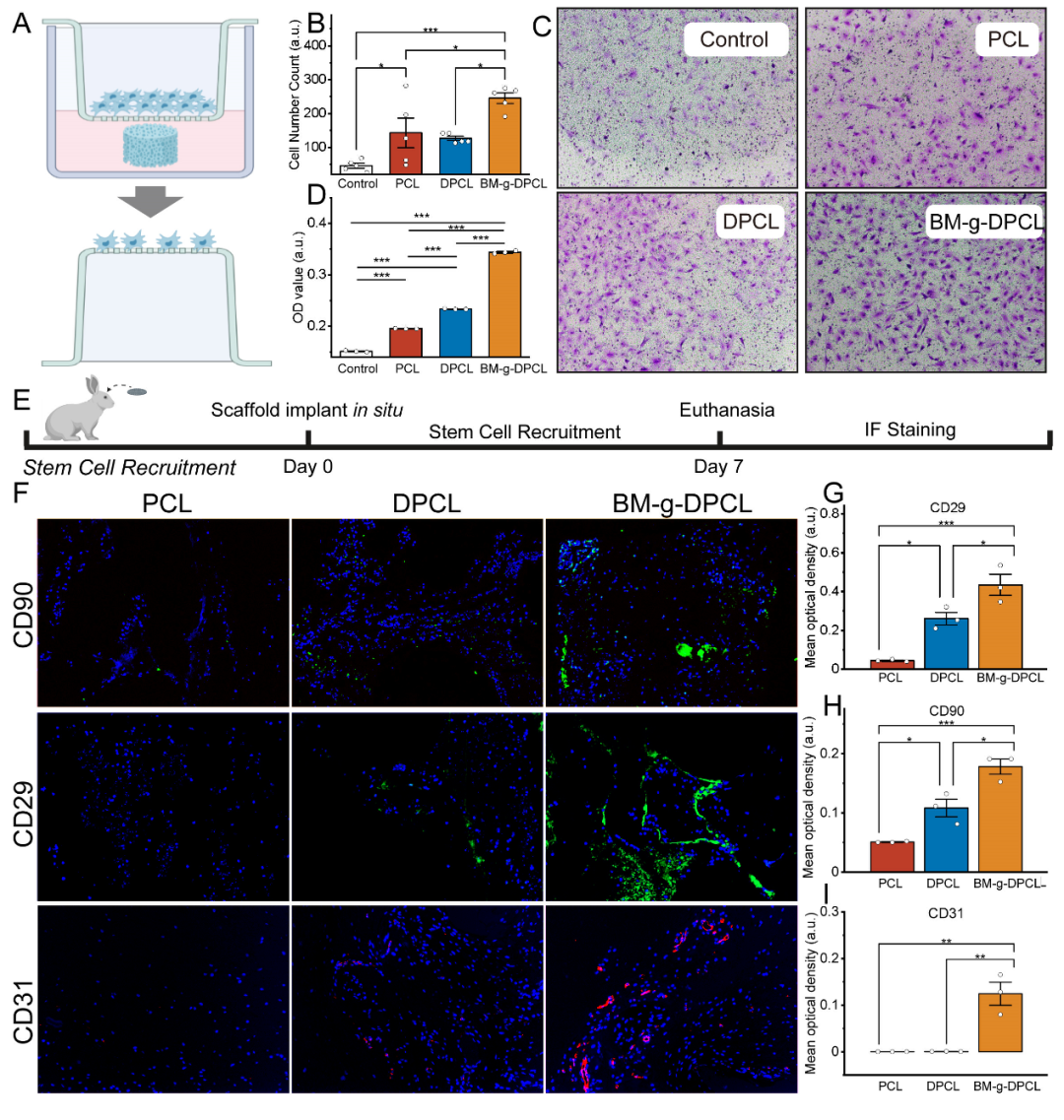
图2 仿生基质加速rBMSCs体外迁移和体内内源性干细胞(ESCs)募集
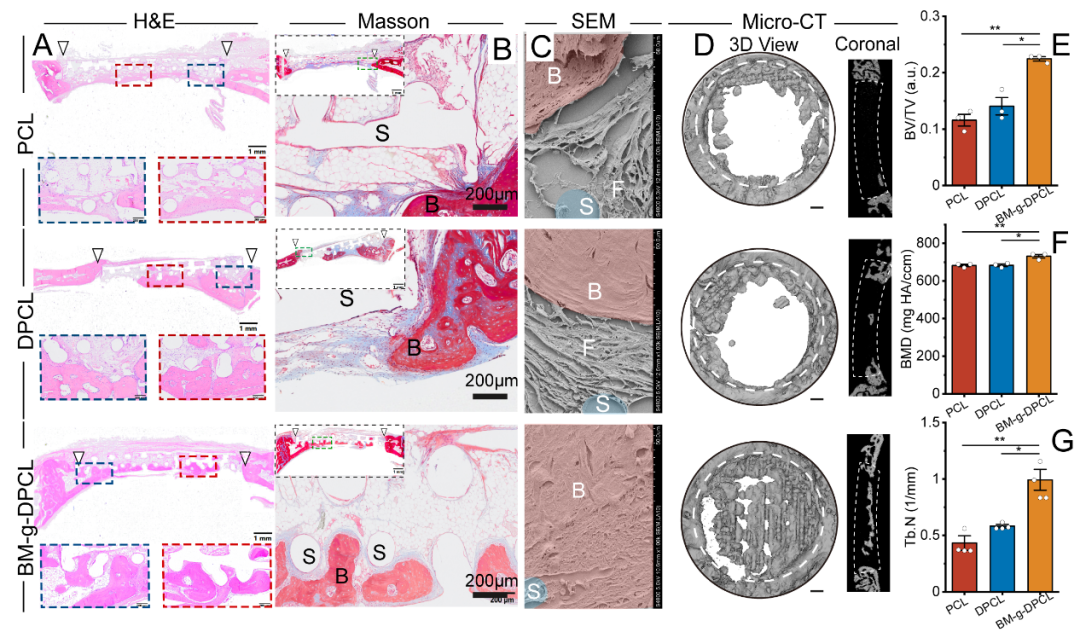
图3 兔临界颅骨缺损的内源性骨再生
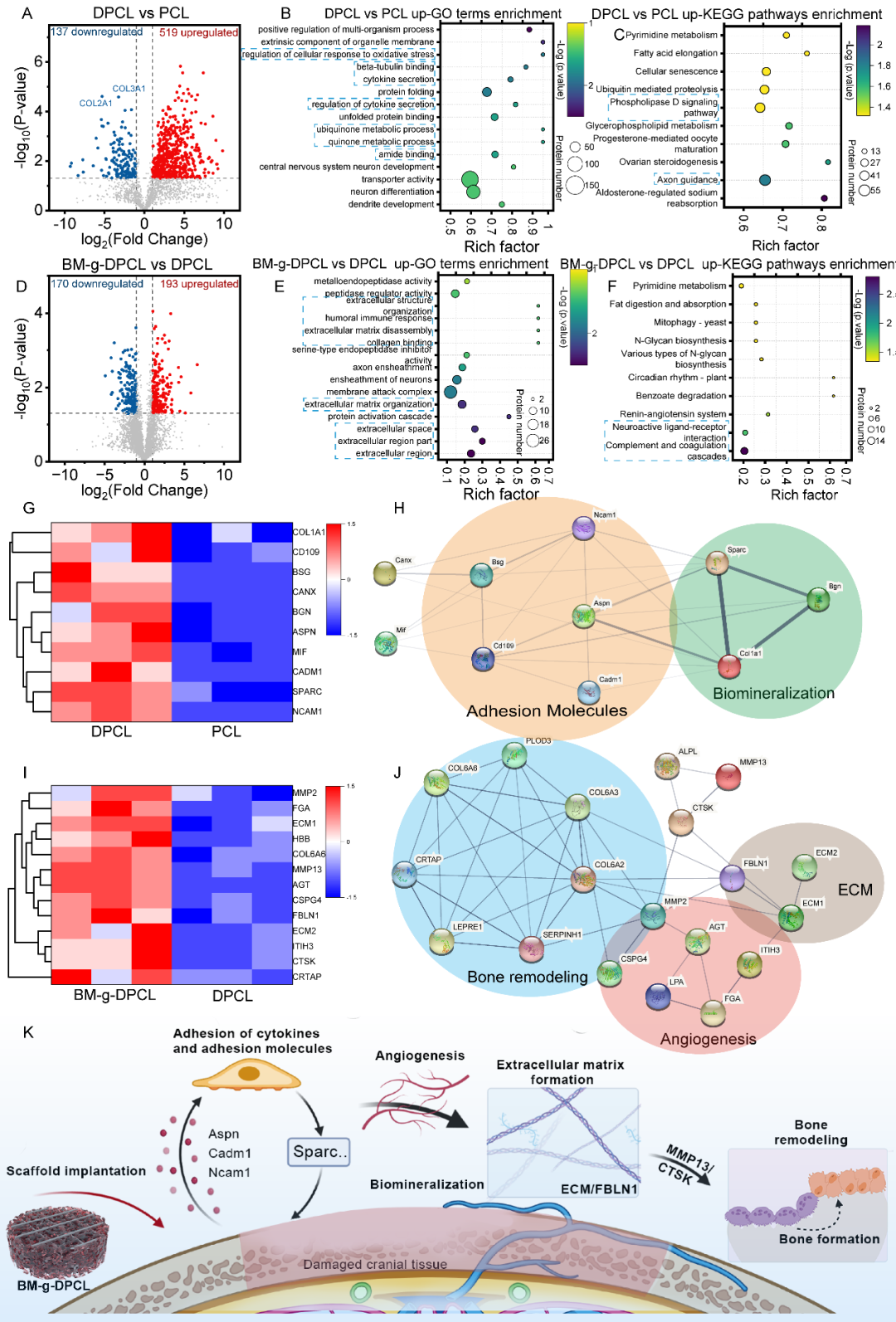
图4 差异的蛋白表达揭示成骨分化机制
研究工作受到国家自然科学基金项目 (Nos. 32271419;32071352) 和四川省重点研发项目 (No. 2020YFS0462)支持。
以上文章转载于微信公众号高分子科技,如有侵权,请及时联系我们修改或进行删除。

